软组织钙化



临床病史
年轻男性,20 岁,主要在肌肉附着点处出现强烈的肌关节疼痛,并且肢体主动和被动活动范围受限。
影像学表现
体格检查显示双臂和双腿呈半屈位并伴有关节僵硬,皮肤出现暗色斑块,脱发,烧灼样疼痛,以及上、下肢对称性皮肤变硬(图1和图2)。 个人背景:19岁时曾患溶血性尿毒症综合征并出现脑缺血受累(经对比增强MRI证实),因19号基因突变导致H因子缺乏。现为慢性肾功能衰竭并接受血液透析。 实验室检查:高钙血症;甲状旁腺激素(PTH)、抗酒石酸酸性磷酸酶(TRAP)、肌酸磷酸激酶(CPK)和醛缩酶均正常。FAN、抗DNA抗体、抗SCL70及乳胶试验均为阴性。血管紧张素转化酶(ACE)在正常范围,红细胞沉降率(ESR)36 mm/h。 进行了CT检查(图3至图9)。
病情讨论
四肢、椎旁肌和腰大肌的软组织中出现线状和融合性的钙化,并伴有屈曲挛缩及肾实质变薄等肾病征象。进行了皮肤活检(图10)。
自1997年首次被发现以来,肾源性系统性纤维化(NSF)仅在患有急性或慢性重度肾功能不全或因肝肾综合征导致肾功能障碍的患者中有报告。自从首次描述NSF(先前称为肾源性纤维化性皮肤病)以来,已有超过200例患者被报道。该疾病患者在全身皮肤和结缔组织中出现纤维化。面部通常不受累。皮肤增厚可阻碍关节的屈伸,导致挛缩。此外,患者可能出现其他器官的广泛纤维化。
需要进行皮肤活检以确诊。该病可能导致虚弱或死亡,死亡通常源于因行动不便引发的感染性败血症,或在肺部和膈肌受累时出现通气不足。其病因尚不明确,目前尚无公认的一致有效治疗。已有报告在肾功能恢复后(无论是自行恢复,还是肾移植后,或在包括体外光化学治疗和光疗等免疫调节治疗后)病情会有所改善。
从组织学上看,皮肤病变可见真皮增厚,胶原束深度延伸至浅筋膜。真皮组织黏蛋白染色呈阳性。表达CD34的真皮细胞支持“循环成纤维细胞”源自骨髓并在发病中发挥作用的概念。基于病理和实验室特征的组合,可将NSF与其他相似疾病(包括系统性硬皮病、黏液水肿症和嗜酸性血管炎)区分开来。其特点包括缺乏抗scl-70和抗着丝点抗体,并且血清电泳结果正常。血管疾病、血栓事件、慢性肝病以及抗磷脂抗体的存在虽与NSF相关,但并未被证实在其发病机制中起到决定性作用。
自1998年以来,为了避免使用碘造影剂或在肾移植前进行检查,在既有肾功能衰竭(ERF)人群中对钆增强磁共振成像的使用日益增多,与NSF患者的报道数量呈现平行关系。Collidge等人1发现,在ERF人群中,使用基于钆的对比剂与NSF的发生存在正相关性,并且所使用的钆喷酸胺(gadodiamide)累积剂量及给药事件也与之呈正相关。对于每一位放射科医师来说,了解该疾病是义不容辞的责任,以避免使易感人群面临风险。
鉴别诊断列表
最终诊断
肾源性系统性纤维化 (NSF)
证书
没有可翻译的英文内容。
图像分析
体格检查

皮肤病变

计算机断层扫描

皮肤活检。HE组织学检查。

第1次CT检查
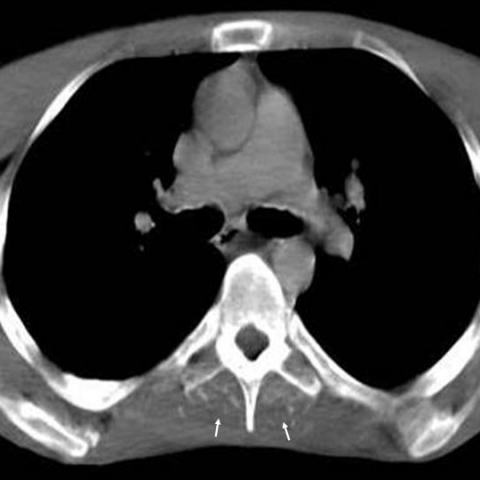
第2次CT扫描

第3次CT扫描

第4次CT扫描

第5次计算机断层扫描
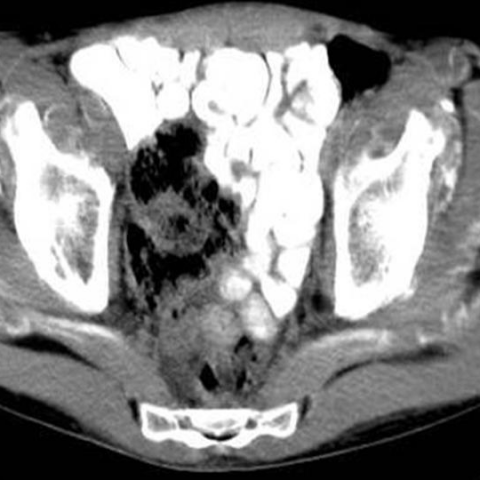
第6次CT扫描

医学影像分析报告
一、影像学发现
患者为 20 岁青年男性,有严重的肌肉及关节疼痛,主要位于肌肉附着处,并伴随四肢关节活动度(主动及被动)受限。结合所提供 CT 及相关影像,可见以下主要特点:
- 软组织内(包括四肢、椎旁肌群及腰大肌区)出现呈线状或融合状的钙化影,范围较广泛。
- 累及肌肉、筋膜及皮下组织,部分区域可见软组织增厚或钙盐沉积,与影像学上较典型的纤维化、钙化改变相匹配。
- 患者肾脏实质出现变薄,提示可能存在慢性肾功能损害。
- 四肢关节可观察到一定程度的屈曲挛缩,提示软组织与肌腱的挛缩或纤维化。
- 皮肤病理切片(图示)表现为真皮层增厚、胶原纤维束异常分布深入浅筋膜,并伴随真皮黏液沉积。
二、潜在诊断
结合临床症状(肌肉-关节强直、疼痛、活动受限)、影像表现(广泛软组织纤维化或钙化)、皮肤活检结果(真皮和浅筋膜纤维化及黏液沉积)以及肾功能不全背景,需考虑以下可能诊断或鉴别诊断:
- 肾源性系统性纤维化(Nephrogenic Systemic Fibrosis,NSF)
原因:多见于急性或慢性严重肾脏功能不全患者,可能与含钆对比剂暴露相关。临床和病理特点包括皮肤增厚、挛缩以及可能波及内脏。皮肤活检可见真皮及筋膜纤维化、CD34阳性细胞增多和黏液沉积。 - 系统性硬皮病(Systemic Sclerosis / Scleroderma)
原因:结缔组织病的一种,可出现皮肤增厚、关节挛缩,但往往伴有免疫学指标(如抗Scl-70或抗着丝点抗体)的阳性,且面部常受累。 - 钙质沉着性肌腱炎或广泛性钙化(如假性痛风、钙化性肌腱炎)
原因:在慢性肾功能不全患者中可能出现广泛性钙磷代谢紊乱,但通常不会表现如此明显的纤维化和深层组织受累。 - 硬皮病样钙质沉积症(Calcinosis Cutis)
原因:可能见于结缔组织病或代谢异常,主要表现为皮肤或皮下组织钙化,但较少出现如本例大面积的挛缩与深部筋膜明显纤维化。
三、最可能的最终诊断
基于本例患者:
- 多处软组织纤维化和钙化,范围涉及四肢、躯干、腰大肌、椎旁肌群。
- 存在明确的肾脏功能受损表现(肾实质变薄)。
- 皮肤组织活检符合真皮与浅筋膜胶原纤维增生及黏液沉积,并无特异性自身抗体(如抗Scl-70、抗着丝点等)的迹象。
- 临床关节活动受限、进行性挛缩。
结合上述特点,最可能的最终诊断是“肾源性系统性纤维化(Nephrogenic Systemic Fibrosis,NSF)”。
四、治疗方案与康复计划
1. 治疗策略
- 改善或恢复肾功能: 如果可能,通过积极治疗原发肾脏疾病(包括血液透析、肾移植等),有助于改善全身症状。
- 避免或谨慎使用钆对比剂: 对有肾功能不全的患者,应严格评估使用钆基对比剂的风险,必要时采用其他检查方法。
- 免疫或调节治疗: 部分患者可尝试糖皮质激素、免疫抑制剂,以及光化学疗法(如体外光化学疗法)、紫外线照射治疗等,但疗效目前尚不完全确定。
- 对症支持治疗: 包括镇痛、营养支持、关节活动度维护等。
2. 康复与运动处方
康复训练的目标在于减轻关节和软组织挛缩,维持肌力和功能,提高生活质量。需根据患者病情、肾功能、心肺功能及对治疗的耐受性应用循序渐进的运动原则(FITT-VP 原则)。
- 频度(Frequency): 初始阶段每周 2~3 次,视耐受情况可逐渐增加至每周 3~5 次。
- 强度(Intensity):
- 低至中等强度为宜,避免过量运动导致疲劳和软组织损伤。
- 可使用简单的关节活动度练习(如关节屈伸、抬举等),并辅以等长或低负荷阻力训练。
- 时间(Time): 每次 15~30 分钟起步,可根据适应情况逐渐延长,避免过度。
- 方式(Type):
- 早期以关节松动、被动牵伸和缓和的肌力训练为主。
- 症状改善后加入简单的有氧训练(如平地快走、骑固定脚踏车等)。
- 进阶(Progression): 在症状缓解和运动耐受度提高后,逐步增加运动时间或轻度增加阻力,强调小步增强原则。
- 体量(Volume)与个体化调整(V – Volume & P – Pattern/individualization):
- 综合考虑患者疼痛程度、关节活动度受限情况,每周有氧训练不宜超过 90~150 分钟,阻力训练强度可根据肌力评估进行调整。
- 注意动态评估患者肾功能及电解质平衡,若出现明显水肿、疲乏或关节疼痛加重,应及时调整康复计划。
对于本例患者,重点在于避免诱发新的软组织损伤及进一步关节活动度丧失。在开始康复训练前,应进行充分的评估与热身,以减少挛缩和粘连带来的疼痛和损伤风险。
安全注意:由于患者存在肾功能不全,需特别关注运动后液体与电解质平衡,避免剧烈高强度训练,并密切监测关节和皮肤的病变进展。
免责声明:
本报告仅为基于所提供材料的参考性医学分析,不可替代面对面就诊或专业医生的诊断及治疗意见。如有疑问或症状加重,建议及时至医院专科就诊。
人类医生最终诊断
肾源性系统性纤维化 (NSF)