肩胛骨软骨肉瘤



临床病史
病人主诉左肩酸痛。肩部X线检查显示异常,提示需进一步进行骨骼显像和MR成像评估。
影像学表现
患者因左肩酸痛就诊。肩部X线检查显示异常,促使进一步进行骨骼显像和MR成像。
X线检查(图1A)发现一个溶骨性病变,伴有爆米花样钙化及硬化边缘,大小约3.5 x 4.1 cm,累及肩胛骨中下部。骨骼显像(图1B)在肩胛骨内侧缘显示局灶性摄取增高。MR成像显示该病变呈环形与弧形对比增强、皮质破坏,并具有与软骨样基质一致的信号特征(图1C)。
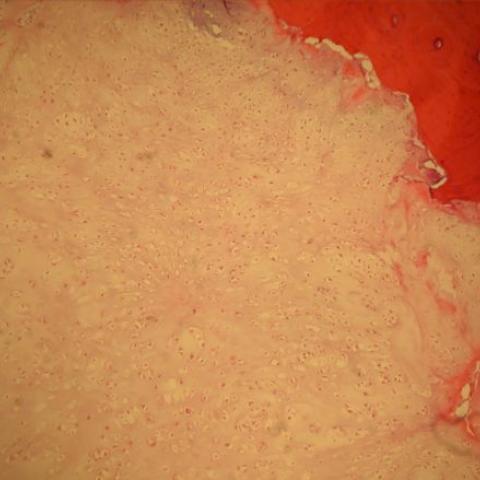
患者接受了部分肩胛骨切除术以切除肿瘤。肉眼观察可见肿块累及皮质骨并似乎延伸至邻近软组织。肿块中心附近可见致密、不规则的钙化。组织病理学检查(图1D)显示,该软骨性肿瘤具有小叶状结构,软骨样基质保存良好,细胞密度不等。大多数细胞形态均一,核深染,未见明显核多形性或有丝分裂像。还可见渗透性生长模式并局部侵犯皮质骨。
病情讨论
软骨肉瘤是由软骨形成细胞构成的恶性肿瘤,同时也是第三常见的骨原发性恶性肿瘤。它们是肩胛骨最常见的恶性肿瘤,既可原发于骨,也可由既存的内生软骨瘤或外生骨疣继发而来。大多数肩胛骨软骨肉瘤患者会以肩部疼痛为首发症状。软骨肉瘤也可由其他已存在的病变继发形成,包括内生软骨瘤、骨软骨瘤、Paget病以及纤维性骨炎。原发性软骨肉瘤可以分为常规型髓内软骨肉瘤、透明细胞型、皮质旁型、黏液型、间充质型、骨外软骨肉瘤以及去分化型。常规型最为常见,大多数病例累及骨干或骨盆 (1)。
放射学检查通常显示溶骨性、偶有膨胀性的病变,外观可类似动脉瘤样骨囊肿或巨细胞瘤(真正的动脉瘤样骨囊肿通常发生在更年轻的年龄组,而且不含爆米花样钙化)。在软骨肉瘤中常可见骨膜反应,这提示了较具侵袭性的过程。软骨肉瘤典型地会出现环形和弧形或爆米花样钙化,可在放射学和断层影像上观察到。一般而言,高级别的病变会导致皮质骨破坏、深层骨内窝蚀,并可向软组织扩展。骨显像通常显示放射性摄取增高。在MR成像中,钙化在所有脉冲序列上均表现为低信号,而软骨基质则表现为T2高信号、T1低信号区,反映透明软骨中水分含量高 (2)。高级别软骨肉瘤在MRI上的表现往往更具多样性。去分化型软骨肉瘤则不会出现软骨样基质典型的小叶状表现。低级别软骨肉瘤与内生软骨瘤之间的鉴别一直颇为困难。然而,Geirnaerdt等人的一项最新研究认为,早期及指数式增强模式的结合与恶性软骨形成性肿瘤显著相关 (3)。
组织学上,软骨肉瘤细胞常具有双核并伴有黏液样区域。浸润性边界及对软组织的侵袭是其典型特征,可帮助区分软骨肉瘤与内生软骨瘤 (4)。
为进行手术规划,需要进行局部分期以显示肿瘤相对于解剖标志的范围。标准治疗方式是手术切除,并尽可能保留较宽的手术切缘;对I级软骨肉瘤而言,保肢性切除术预后良好。当I级软骨肉瘤复发时,通常会将其视为高级别病变 (5)。
鉴别诊断列表
最终诊断
肩胛骨低度恶性软骨肉瘤
证书
(无内容可翻译)
图像分析
肩胛骨的常规X线检查

骨骼闪烁显像

肩胛骨磁共振成像

组织学
医学分析报告
一、影像学发现
1. X 光片(左肩部):可见肩胛骨内出现一处边界相对清晰但具有局部侵蚀性改变的肿物影,局部可见“环形”或“爆米花样”钙化影,提示钙化软骨基质。
2. 骨扫描:左肩部对应区域放射性核素摄取增高,提示局部代谢活跃的病变或肿瘤性病变。
3. 磁共振成像(MRI):病灶在T2加权像上呈明显高信号,T1加权像上呈中低信号,可见局部软骨样基质,部分钙化区域在各序列上信号减低;有一定程度的皮质破坏并可见轻微软组织受累。整体影像学表现提示软骨样肿瘤且具有一定侵袭性特点。
二、潜在诊断
- 软骨肉瘤(Chondrosarcoma):
根据肩胛骨部位易发生软骨肉瘤,以及影像上“环形”或“爆米花样”钙化、肿瘤扩张并伴皮质破坏等特点,软骨肉瘤是首要考虑。 - 内生软骨瘤(Enchondroma):
也可在骨内出现软骨样病变和钙化,但通常生物学活性较低,侵袭性相对较小,无明显皮质破坏或软组织肿块。 - 动脉瘤样骨囊肿(ABC):
影像学上常为膨胀性、囊性病变,患者年龄偏年轻,但其钙化特点并不突出“软骨样钙化”;与本病在影像上有一定重叠,但钙化表现并不典型。 - 巨细胞瘤(Giant Cell Tumor):
常见于骨骺闭合后年轻人,发生在长骨干骺端附近;然而其无显著软骨样钙化,并多位于长骨端部,加之影像学形态学并不完全相符。
三、最终诊断
综合患者年龄(19岁)、肩胛骨部位、临床症状(左肩疼痛)、影像学表现(典型软骨样钙化、侵袭性改变)以及组织病理(双核软骨细胞、软骨基质伴黏液样变等特征),最可能的诊断为:肩胛骨软骨肉瘤(Chondrosarcoma)。
四、治疗方案与康复计划
1. 治疗策略:
(1)手术治疗:标准治疗方式为广泛或边缘扩大切除,尽可能保留肩关节及肩带功能,必要时可行肩胛骨部分切除并重建。
(2)辅助治疗:对于高分级或局部侵袭明显者,可考虑术后放疗或化疗,但对于多数低分级软骨肉瘤而言,手术切除是主要手段,放化疗的作用有限。
(3)随访:定期随访影像学评估术后复发或远处转移情况,尤其在首5年需密切观察。
2. 康复/运动处方建议:
手术恢复后,根据病变范围及肌力情况,逐步进行肩关节和上肢功能训练。需要注意软骨肉瘤术后创面及可能的重建假体或敷料支撑,确保肩关节稳定性。遵循FITT-VP原则:
- 频率(Frequency):术后早期每日进行1-2次关节活动度与轻度肌力训练,3-4周后逐渐增至每周3-5次。
- 强度(Intensity):初期以低阻力、低负荷练习为主,防止牵拉痛或造成关节不稳;根据肌力与疼痛程度逐渐增加阻力。
- 时间(Time):每次康复训练时间由10-15分钟逐渐延长至30分钟或以上,分组进行;避免长时间持续训练。
- 方式(Type):从被动关节活动逐渐过渡到主动活动,配合弹力带和轻量哑铃训练;结合肩关节周围肌肉的等长收缩、等张收缩等多种练习方式。
- 进阶(Progression):随着关节活动度与肌肉耐力的提高,逐渐增加活动幅度与负重量,后期可配合游泳、划船机等低冲击活动,保护肩关节稳定。
- 体积(Volume):在确保安全前提下,逐步增加训练组数与重复次数,切忌一次性过度训练造成疲劳或再损伤。
在康复过程中,应密切关注伤口愈合、疼痛及关节活动度变化。如有明显疼痛加重、肿胀或功能下降,应及时就诊评估。
免责声明:本报告仅基于现有影像与初步病理信息作出参考性分析,不能替代面对面诊疗或专业医生意见。具体治疗和康复方案应由主治医师结合患者实际情况综合制定。
人类医生最终诊断
肩胛骨低度恶性软骨肉瘤