骨母细胞瘤样骨肉瘤在桡骨远端的局部复发



临床病史
一名29岁女性,曾患右桡骨骨成骨细胞瘤,并接受过瘤内刮除术治疗。三年后,她因在腕关节活动时出现反复疼痛而再次到骨科就诊。
影像学表现
X射线成像显示手术区域周围出现新的溶骨性病变。磁共振成像(MRI)显示在远端干骺端出现多处新发病灶的局部复发,这些病灶在T1加权像(T1W)上为低信号、在T2加权像(T2W)上为高信号,并在中心呈对比增强。影像学特征提示这些病灶可能是骨母细胞瘤向低级别肉瘤发生去分化并伴有跳跃性病灶,或者是骨母细胞瘤的局部复发伴周围的骨母细胞瘤样病变(图1、2、3)。为进行分期,进行了正电子发射断层扫描和计算机断层扫描(PET/CT)检查,结果显示仅在桡骨远端病灶处有代谢活性(SUV最大值4.2)(图4)。患者接受了桡骨远端的大范围外科切除、尺骨移位重建以及关节融合手术(图5)。组织学检查结果将该病灶确认为1级骨母细胞瘤样骨肉瘤(OBLOS)。
病情讨论
OBLOS是一种常规骨肉瘤(OS)的罕见变异类型,占所有骨肉瘤的1.1% [1, 2]。它主要影响年轻成年人,男性与女性的患病比例略高(1.2:1)[1, 3]。它在受累部位引起慢性进行性疼痛,并伴有肿胀以及邻近关节活动度降低[1, 3-5]。由于其临床表现以及组织学和放射学表现相似,OBLOS与良性成骨细胞瘤(OB)难以区分。与OB不同的是,OBLOS具有转移能力,并且死亡风险较高[3]。OBLOS常见的发病部位为长骨的干骺端,最常见于胫骨,其次是椎骨、手、足以及股骨[1]。
常规放射学影像通常显示病灶呈溶骨性,周围骨皮质变薄并且皮质破坏,或者表现为界限清晰的病灶,伴有硬化边缘[1, 3]。MRI扫描是评估骨髓腔和软组织受累范围的可靠诊断工具。病灶在T1加权像上呈低信号,在T2加权像上呈等或高信号,并伴有明显的骨髓水肿。扫描往往可见中心不连续的对比增强。然而,MRI扫描并无定论,因为良性病变也可能表现出侵袭性[1, 3, 6]。在组织学上,OBLOS与成骨细胞瘤较为相似,有时唯一的区别在于OBLOS具有更高的有丝分裂活性(包括异常有丝分裂)并呈浸润性生长,而成骨细胞瘤则不具备这些特征。在分子遗传学层面,超过90%的成骨性骨瘤和成骨细胞瘤可检测到FOS或FOSB基因易位,而骨肉瘤中尚未发现此类基因易位[7, 8]。
本病例中,对切除的桡骨远端进行组织病理学检查,发现了七个独立的成骨细胞增生灶,形态上类似于多发性成骨性骨瘤/成骨细胞瘤的瘤巢,但局部可见浸润性生长并且有丝分裂活性增高(Fig. 6),其中包括一些异常有丝分裂。分子遗传学检测同时显示FOS或FOSB基因并无易位。因此,组织学诊断更倾向于1级类似成骨细胞瘤的骨肉瘤(OBLOS),而非成骨细胞瘤病。
由于OBLOS具有转移能力,预后不佳,转移多见于肺部,偶见于骨骼[4, 9, 10]。广泛外科切除联合化疗通常是首选的治疗方案[9, 11]。
我们报告这一例OBLOS以强调其与良性病变之间的鉴别有多么困难。错误的诊断可能导致手术治疗不足并导致局部复发。临床医生应加大随访频率。
已获得患者的书面知情同意用于发表。
鉴别诊断列表
最终诊断
成骨细胞瘤样骨肉瘤
图像分析
初次入院时的前后位X线片

初次入院时的MRI扫描


第一次治疗后三年的MRI扫描



治疗后三年的FDG PET-CT骨扫描

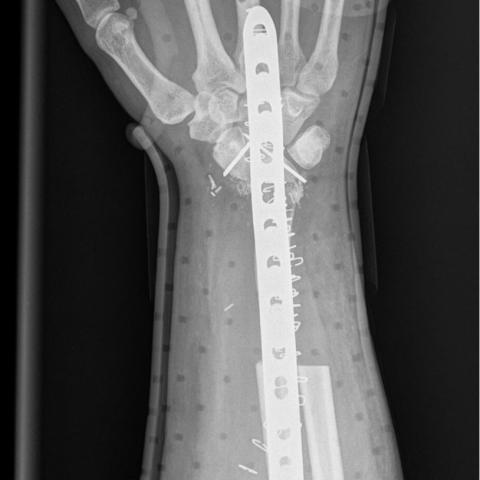
手术切除后右腕的前后位X线片
大体切除及组织病理学图像



医学分析报告
一、影像学发现
根据提供的X线和MRI影像,可见右桡骨远端存在多个类似“成骨性病灶”的改变,病灶区存在以下特点:
- 在X线片上:可见桡骨远端有边界相对清晰的骨质破坏区,部分区域伴有骨皮质变薄、局部骨质硬化或破坏,并出现不同程度的骨质增生征象。
- 在MRI序列上:病灶在T1加权像上显示低或稍低信号,在T2加权像上显示等或稍高信号,局部可见骨髓水肿信号。强化扫描显示病灶内不均匀或分散的强化表现,提示存在活跃的成骨或肿瘤细胞增殖。
- 影像上可见多处“结节状”或“团块状”病变灶,部分病变延伸至软组织附近,但以骨内改变为主。
- 结合既往病史,局部可见手术后改变(钉板固定及局部缺损修复迹象)。
总体而言,影像学表现提示右桡骨远端存在多发性骨质破坏伴新生骨形成征象,需结合病史和病理学进一步综合判断。
二、潜在诊断
基于以上影像学表现以及患者既往右桡骨骨肿瘤病史,考虑以下可能性:
- 良性骨肿瘤/肿瘤样病变(如复发的骨母细胞瘤,Osteoblastoma):
原有的病变为骨母细胞瘤,复发时可出现类似的成骨病灶,影像学上亦可表现为骨质破坏及骨质增生相混杂,且可有反复疼痛症状。 - 恶性成骨性肿瘤(如成骨肉瘤,Osteosarcoma,包括骨母细胞瘤样成骨肉瘤):
成骨肉瘤可表现为侵袭性骨质破坏和肿瘤新骨形成,不均匀强化及局部疼痛。在有骨母细胞瘤既往病史时,后续出现更具侵袭性的病灶需高度警惕这类恶性病变。 - 其他罕见成骨性病变:
如骨软骨瘤或其他骨肿瘤亚型,但结合患者病史和影像表现,可能性相对较低。
三、最终诊断
结合患者年龄、症状、既往骨母细胞瘤病史、此次影像学表现以及病理及基因检测结果(FOS/FOSB基因阴性,组织学上见局部侵袭性生长及异常有丝分裂)等综合信息,最可能的诊断为:
骨母细胞瘤样成骨肉瘤(Osteoblastoma-like Osteosarcoma,简称OBLOS)
该病虽与骨母细胞瘤在部分组织学和影像学方面有相似之处,但其更具侵袭性和转移潜能,因此在最终诊断和后续治疗上应予以高度重视。
四、治疗方案与康复计划
基于骨母细胞瘤样成骨肉瘤的恶性程度及其潜在的转移风险,通常治疗策略包括:
- 外科治疗:推荐行广泛或扩大切除以保证肿瘤边界干净。对于已行局部刮除但复发的病例,可能需要更大范围的骨切除或重建。
- 化疗:成骨肉瘤相关的术前或术后辅助化疗可降低远处转移率,提高长期生存率。具体方案需根据肿瘤分期、病理分级和患者整体情况由肿瘤专科医生制定。
随着治疗结束后,患者仍需定期随访评估治疗效果及排除复发或转移。康复训练对恢复腕关节功能至关重要:
- 早期康复(术后0-6周):
- 在保证内固定或外保护装置稳定的前提下,可做轻度肌力和关节活动度练习,如手指屈伸活动、腕关节被动活动等。
- 频率可为每天2-3次,每次5-10分钟,强度轻盈,避免疼痛加剧。
- 中期康复(术后6-12周):
- 逐步增加主动关节活动度训练,例如自主的腕关节前屈、背伸以及旋前旋后动作。
- 可在医生或治疗师指导下进行弹力带或轻重量的抗阻训练,增强前臂肌群力量。每周可安排3-4次,每次15-20分钟。
- 后期康复(术后12周及以后):
- 进一步加强力量和灵活度训练,增加腕关节稳定性及运动协调性,如小球抓握、腕关节绕圈运动等。
- 根据耐受程度,可逐步恢复日常生活和轻体力劳动,后期再考虑逐渐回到较高强度或运动项目。
注:整个康复过程需遵循FITT-VP(频率Frequency、强度Intensity、时间Time、类型Type、体积Volume、进度Progression)原则,应根据个人具体情况逐步调整。若出现明显疼痛、肿胀或其他不适,应及时就医或与康复师沟通。
五、免责声明
本报告仅基于现有病历及影像资料所作参考性分析,不能替代面对面诊疗及专业医生意见。若有任何疑问或症状变化,请及时就诊,以获取个体化的治疗与康复方案。
人类医生最终诊断
成骨细胞瘤样骨肉瘤