周围神经鞘瘤伪装成骨肿瘤


临床病史
一名44岁的男性患者,因左肩机械性疼痛持续数月就诊。体格检查显示关节活动度和肌力均保持良好。患者既往病史无特殊。
影像学表现
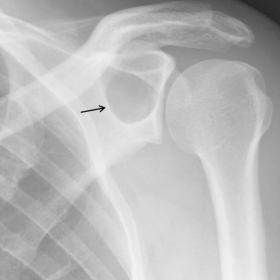
前后位放射影像显示肩胛骨存在一处边界清晰的溶骨性病变。该病变具有狭窄的过渡带及薄薄的硬化缘。未见皮质破坏、骨膜反应或基质形成。(Figure 1)
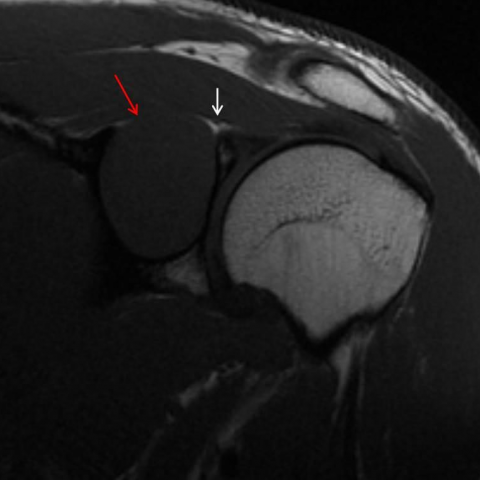
磁共振成像(MRI)检查证实在肩胛盂棘切迹处出现一个实体、圆形且边界非常清晰的软组织肿块(3.5 x 2.8 x 2.4 cm)。同时,可见肩胛骨也出现大范围重塑,但保留了一层非常薄的残余皮质。
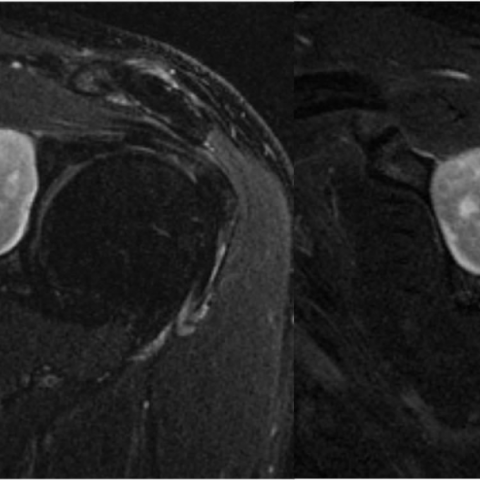
该病变在T1加权像(WI)上呈中等信号强度(Figure 2),在T2加权像(WI)上呈高信号强度(Figures 3),并在注射钆剂后均匀强化(Figure 4)。
可见肿瘤与肩胛上神经之间关系密切,但尚未明确显示两者的直接相连(Figure 2)。
未见提示去神经支配的肌肉萎缩、脂肪浸润或水肿的证据。
CT引导下穿刺活检结果确诊为神经鞘瘤(Figure 5)。
病情讨论
单发良性周围神经鞘肿瘤可分为施万细胞瘤(neurilemmoma)和神经纤维瘤。
在多达 90% 的病例中,施万细胞瘤和神经纤维瘤均为单发病灶,与 1 型神经纤维瘤病无关。另一方面,1 型神经纤维瘤病几乎总是出现多个神经纤维瘤,累及内脏和深部神经,并且恶性转化风险增加。
施万细胞瘤主要由施万细胞组成,相对于受累神经呈偏心分布,具有由外神经膜构成的真正包膜;通常可以与下方神经纤维分离。
相反,神经纤维瘤为居中分布,极少有包膜,且无法与神经分离 [1, 2]。
施万细胞瘤常见于 20–40 岁的患者,约占良性软组织肿瘤的 5%。它们通常表现为无痛、缓慢生长的软组织肿块,只有当病变增大到足以压迫邻近神经时,才可能出现症状 [1]。
在 MRI 上,施万细胞瘤表现为 T1-WI 等或低信号、T2-WI 高信号,并具有明显的对比增强。
病灶通常呈梭形,纵向排列,两端逐渐变细并与其起源的神经相连。
病灶在 T2-WI 上可呈现典型的“靶征”:即中心低信号区域;也可出现“分脂征”(split-fat sign),代表肿瘤边缘周围的一圈脂肪,尤其在肌间隙位置时更明显。
在许多情况下,仅凭影像学难以区分施万细胞瘤和神经纤维瘤,两种肿瘤都可能呈梭形外观,并出现“分脂征”或“靶征” [3]。
当施万细胞瘤与骨骼紧密相邻时,往往难以判断它是累及骨骼的软组织施万细胞瘤,还是累及周围软组织的骨内施万细胞瘤 [4],但后者较罕见。本例中,肿瘤由于缓慢生长而导致继发性骨重塑。
手术切除是治疗施万细胞瘤的首选方式,病灶通常可与原发神经分离,从而保留其他神经纤维及其功能。复发罕见,恶性转化极其罕见 [1]。
要点提示:
由于软组织施万细胞瘤与骨骼邻近且生长缓慢,可能表现为良性骨单发病灶。对于任何与神经紧密相关且边界清晰的肿块,都应将周围神经鞘肿瘤列入鉴别诊断。
鉴别诊断列表
最终诊断
肩胛上神经分支的神经鞘瘤,表现类似骨肿瘤。
图像分析
前后位X线平片

斜冠状位 T1加权像
轴向及斜冠状位 T1脂肪抑制加权成像配合静脉注射钆增强剂

轴向CT

斜冠状面和矢状面 T2 脂肪抑制加权成像
医学影像分析报告
一、影像学发现
通过对左肩部X线与MRI影像的综合评估,可观察到肩胛骨近关节区域(肩峰下或关节盂附近)存在一处边界清晰的软组织肿物。X线示该肿物导致邻近肩胛骨呈明显“压迫”或“改建”,可见局部骨质变薄或轻度膨隆性改变,提示病变生长缓慢,对骨质产生长期的推压效应。
MRI平扫及增强扫描显示:
1. 在T1加权像(T1WI)上肿物表现为与肌肉等信号或略低信号。
2. 在T2加权像(T2WI)上呈高信号,可见“靶征”(target sign)或“分脂征”(split-fat sign,即肿物周围可见脂肪带)。
3. 增强扫描后肿物呈显著强化,呈梭形或近圆形,与周围软组织分界较清。
4. 肿物位置与神经通道关系密切,但观察到大部分神经纤维并未被完全侵犯,可见肿物在神经束一侧偏心性生长。
5. 病灶生长缓慢,未见明显侵蚀性改变或软组织破坏。
二、潜在诊断
-
1. 神经鞘瘤(Schwannoma):
基于影像表现(T2高信号、可见靶征或分脂征、偏心性生长)以及患者症状(缓慢进展、机械性疼痛),周围神经鞘瘤是主要考虑的良性周围神经鞘肿瘤之一。该病常见于20-40岁人群,也可出现于40多岁,常表现为无痛性或轻度疼痛性肿块,随着肿物增大可出现神经受压症状。 -
2. 神经纤维瘤(Neurofibroma):
同样属于周围神经鞘肿瘤,在影像上与神经鞘瘤相似,也会出现T2高信号及“靶征”。但神经纤维瘤多为中心性生长,且常不易与神经纤维分离。如患者无神经纤维瘤病(NF1)的其他特征,且本例肿瘤有包膜,偏心性,较易与神经纤维分离,更倾向于神经鞘瘤。 -
3. 其他软组织肿瘤:
如脂肪瘤、血管瘤或其他罕见软组织良性肿瘤,可呈慢性生长,但通常MRI信号与本例不同(如脂肪瘤在T1WI和T2WI上呈高信号并可抑脂)。且本例与神经走行关系密切,更符合神经源性肿瘤。
三、最终诊断
结合患者年龄(44岁)、症状(慢性左肩机械性疼痛)、影像所示的软组织肿块形态(包膜完整、偏心性、易于与神经纤维分离、T2高信号并显著强化)以及术中或活检病理可确认,小结如下:
最可能的诊断:神经鞘瘤(Schwannoma,良性周围神经鞘瘤)。
若仍需获得最终确诊,可行手术切除并进行病理学检查,以排除其他罕见类型的神经源性或软组织肿瘤。
四、治疗方案与康复计划
-
手术治疗:
对于大多数惰性生长但导致症状或有潜在神经受压的神经鞘瘤,手术彻底切除是首选方案。由于神经鞘瘤通常与原发神经束偏心性附着,并有完整包膜,术中可通过显微外科技术在保留神经纤维的同时完整切除肿瘤。 -
术后康复:
- 近期康复(术后1~4周):主要以减轻疼痛和水肿、预防关节僵硬为目的。常规应用冰敷(非开放创口情况下)、合适的肩部支具或三角巾固定(依术式与医嘱而定),并在可耐受范围内进行肩关节被动活动(前屈及外展各方向)等轻柔练习。
- 中期康复(术后4~8周):在疼痛可控后,逐步增加主动活动度练习,例如:手指爬墙动作、弹力带的轻度抗阻练习(外展、内收、前屈等)。避免过度负重及过于剧烈的外力牵拉,循序渐进地增强肩周肌力。
- 后期康复(术后8周及以后):加强肌力与功能性训练,包括肩袖肌群和肩胛稳定肌的抗阻训练,可逐步增加弹力带阻力级别或使用轻质哑铃进行强化。配合改良的日常活动训练(如穿衣、梳头、提轻物等)以恢复肩关节正常功能。
-
运动处方(FITT-VP 原则参考):
- 频率(Frequency):每周3~5次肩关节专项练习,视术后恢复情况可逐步增加至每日适度活动。
- 强度(Intensity):早期以不引发或仅轻度诱发疼痛为宜,中后期逐步提升阻力或重复次数。
- 时间(Time):单次康复训练可持续15~30分钟,并分段进行,避免疲劳性损伤。
- 方式(Type):包括关节活动度训练、轻量阻力练习(弹力带或小哑铃)、本体感觉及肩关节稳定性训练。
- 进阶(Progression):伴随功能恢复,逐渐提高阻力、增加动作数量并进行更复杂的肩关节动作。每步进阶前应确认局部组织愈合与肌群耐受均良好。
如果患者存在骨质疏松、心肺功能不佳或其他合并症,需在专业医护人员的指导下调整训练强度与形式,密切观察术后及康复过程中的不适反应,确保安全。
免责声明:
本报告仅基于当前提供的病史与影像学信息,旨在提供参考性医学分析。具体诊断与治疗方案应结合患者实际情况,由专业临床医生进行线下面诊、综合评估后最终确定。本报告不能替代医生的当面诊断或医疗决策。
人类医生最终诊断
肩胛上神经分支的神经鞘瘤,表现类似骨肿瘤。